Comme pour toute infection virale, le diagnostic biologique de l’infection à SARS-CoV-2 (maladie « COVID-19 ») repose sur la connaissance de la physiopathologie de l’infection et de la cinétique des marqueurs viraux. La figure proposée ci-dessous résume cette cinétique et s’appuie sur les données de la littérature les plus solides et les plus convaincantes.
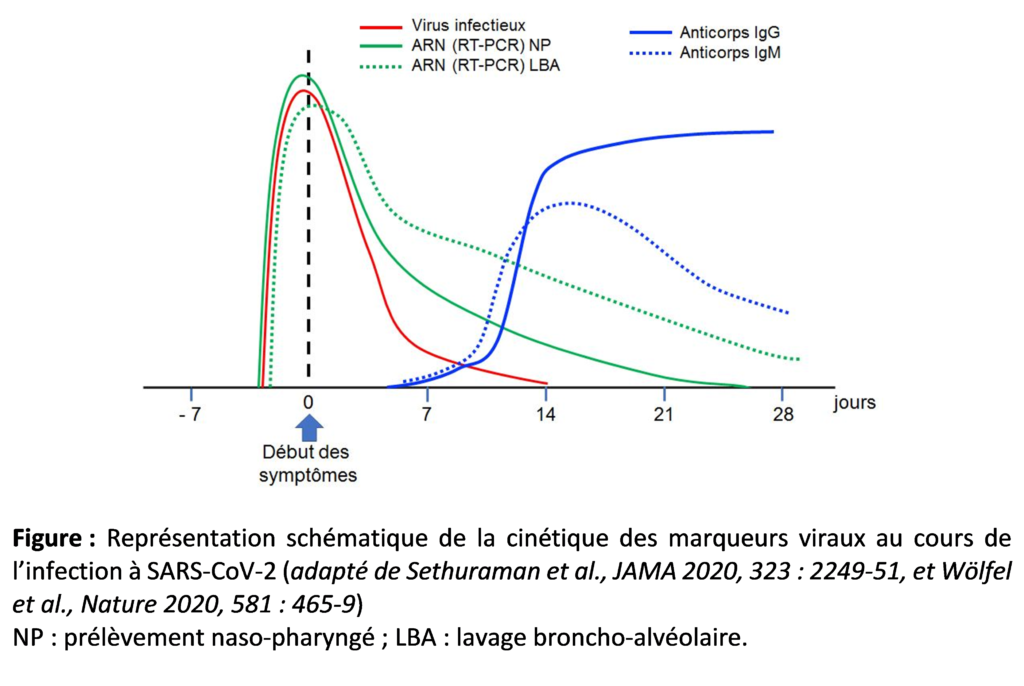
La maladie COVID-19 étant une infection respiratoire à incubation courte (en moyenne 5 jours), le diagnostic de choix est le diagnostic direct: mise en évidence du virus ou de ses constituants, le plus tôt possible après le début des symptômes.
Dès le début de l’épidémie il est apparu que la recherche de l’ARN viral par RT-PCR (amplification génique après rétrotranscription) dans les prélèvements naso-pharyngés était la méthode la plus appropriée. Elle reste la méthode de référence. L’ARN viral y est présent avec une charge virale élevée en moyenne dans les deux jours précédant l’apparition des symptômes et dans les premiers jours suivants. La charge virale diminue alors progressivement mais l’ARN viral peut être détecté pendant plusieurs semaines sans que cette persistance soit liée à l’infectiosité. En effet, l’infectiosité (évaluée par isolement du virus par culture cellulaire) semble très réduite, voire nulle, au-delà de 8 jours après le début des symptômes.
La charge virale est régulièrement plus élevée dans les prélèvements profonds (lavages broncho-alvéolaires, crachats) et l’ARN viral demeure plus facilement détectable dans ces prélèvements au-delà d’une semaine après le début des symptômes. Les prélèvements profonds sont donc à privilégier en cas de diagnostic tardif si suspicion d’infection sévère à SARS-CoV-2. La recherche de l’ARN viral par RT-PCR n’est pas recommandée dans les autres prélèvements : écouvillons oro-pharyngés et salive (moindre performance car charge virale moins élevée), selles (détection inconstante) et sang (virémie quasi-inexistante).
Le diagnostic de masse requiert un équipement relativement lourd pour faire face à un grand nombre de demandes, ce qui explique le délai nécessaire de plusieurs heures pour disposer du résultat. Des tests moléculaires unitaires, dont certains reposent sur un principe d’amplification isotherme, sont disponibles et permettent de disposer d’un résultat rapide (moins d’une heure). Ils ne se prêtent cependant pas au dépistage de masse.
Des tests rapides de détection des antigènes viraux (« TROD », tests antigéniques reposant sur le principe de l’immunochromatographie) sont récemment apparus. Si leur rapidité et leur simplicité sont très attrayantes, leur sensibilité est inférieure à celle de la PCR (sensibilité globale de l’ordre de 60%). Ils ne peuvent donc pas remplacer la PCR mais représentent une alternative dans des situations d’urgence. Ainsi la Haute Autorité de Santé (HAS) autorise leur utilisation pour des patients symptomatiques dans les 4 premiers jours suivant l’apparition des symptômes (période de charge virale élevée) si le test RT-PCR ne peut pas être obtenu sous 48 heures. Leur utilisation est également possible dans le cadre d’opérations de dépistage à large échelle ciblant des populations au sein desquelles le risque d’infection est plus important qu’en population générale (HAS, communiqué du 9 octobre 2020).
Pour ce qui concerne le diagnostic indirect, la détection des anticorps anti-SARS-CoV-2 est optimale seulement à partir de J14 post-début des symptômes (seulement environ 50% de séroconversions entre J7-J11).
La sérologie a un intérêt très limité pour le diagnostic initial : uniquement diagnostic de rattrapage chez des patients symptomatiques (avec ou sans signes de gravité) si tableaux évocateurs d’infection à SARS-CoV-2 avec RT-PCR négative (ou non réalisée dans les 7 jours suivant l’apparition des symptômes). La recherche d’anticorps est alors à effectuer au moins 14 jours après le début des symptômes. La recherche d’IgM spécifiques anti-SARS-CoV-2 au sein d’une sérologie positive n’a pas d’intérêt identifié actuellement. Dans l’état actuel des connaissances, la présence d’anticorps anti-SARS-CoV-2 signe uniquement le contact possible avec le virus. Bien qu’il semble que la présence de ces anticorps soit associée à une activité neutralisante, aucune donnée ne permet aujourd’hui d’affirmer de manière définitive que ces anticorps soient associés à la protection vis-à-vis d’une infection ultérieure ni la durée de cette potentielle protection. De plus, des réactions croisées avec d’autres coronavirus, notamment les coronavirus humains ubiquitaires (229E, OC43, NL63 et HKU1), ne peut pas être exclue.
Francis BARIN
Professeur émérite,
Inserm U1259, Université de Tours









